О.Л.Ивко, Л.Н.Прахова, Т.Л.Цветкова, А.Г.Ильвес, И.Г.Никифорова, А.М.Петров, М.В.Вотинцева,И.Д.Столяров
Рассеянный склероз – демиелинизирующее заболевание ЦНС, наиболее часто поражающее активно работающих людей в возрасте от 15 до 50 лет и приводящее к инвалидизации. Одной из основных причин, ведущей к развитию нетрудоспособности, являются нарушения ходьбы. Походка больных рассеянным склерозом отличается от походки здоровых людей в 35% случаев - уменьшением скорости ходьбы, в 25% случаев - уменьшением в длине шага, в 22% случаев - уменьшением числа шагов в мин, в 23% случаев - увеличением ширины шага [10]. Нарушения ходьбы при рассеянном склерозе чаще всего связаны с поражением пирамидной, мозжечковой систем, расстройствами чувствительности и, более чем у 80% больных, вызваны развитием нижнего спастического парапареза [4].
Под спастичностью понимают зависимое от скорости возрастание сопротивления мышцы (или группы мышц) пассивному растяжению, причем увеличение мышечного сопротивления напрямую зависит от скорости пассивного движения исследуемой конечности [4]. Основными жалобами (связанными с повышенным мышечным тонусом в ногах), которые предъявляют больные, являются: чувство скованности в ногах, быстрая утомляемость, периодические боли и судороги. Физическую активность больного при этом ограничивает не только мышечная слабость, но и выраженное повышение мышечного тонуса. Спастический парез приводит к ограничению объема движений в пораженной конечности, вторичным изменениям в мышцах, суставах и сухожилиях и, как следствие, к контрактурам.
Мышечный гипертонус при рассеянном склерозе носит ряд отличительных особенностей: отмечается нестойкость выраженности мышечной гипертонии (она может носить преходящий характер). Кроме того, имеет место зависимость степени выраженности спастичности от позы больного. При исследовании мышечного тонуса в положении лежа пластический гипертонус часто выражен нерезко, в то время как при ходьбе он значительно нарастает. Урологические заболевания, задержка мочи также могут приводить к усилению синдрома спастичности [8].
Необходимо отметить, что спастичность может играть адаптивную роль. При выраженной степени пареза пациент может использовать конечность как опорную. В таком случае попытка уменьшить спастичность приводит к ухудшению двигательной функции. Поэтому терапия, направленная на коррекцию спастичности, должна быть строго индивидуальной и тщательно мониторируемой.
Для количественной оценки выраженности изменений мышечного тонуса и контроля за проводимой терапией наиболее часто используется модифицированная шкала Эшуорта (Ashworth, 1964). Данный метод не позволяет получить точную количественную информацию о степени ограничения двигательных способностей из-за относительной субъективности: достоверность информации во многом зависит от опыта исследователя.
В клинической практике для коррекции спастичности при рассеянном склерозе наиболее часто используются миорелаксанты с центральным механизмом действия: мидокалм (толперизон), баклофен (лиорезал), сирдалуд (тизанидин). Механизм действия этих препаратов связан с их воздействием на полисинаптические рефлексы, которые участвуют в формировании спастичности, и незначительным влиянием на моносинаптические рефлексы, от которых зависит мышечная сила. Препараты этой группы характеризуются хорошей переносимостью и минимумом побочных эффектов, поэтому они могут быть рекомендованы для длительного приема. Однако, у части пациентов могут развиваться побочные эффекты; чаще они носят дозозависимый характер и проявляются в виде слабости, абдоминального дискомфорта и т.д., что может значительно снижать качество жизни пациентов.
Для диагностики нарушений опорно-двигательного аппарата, планирования процесса реабилитации и оценки эффективности лечебных мероприятий ряд исследователей используют инструментальные методики с регистрацией временных, кинематических, динамических параметров ходьбы и функциональной электромиограммы (ЭМГ) [2]. Наряду с этим, широкое распространение получил также метод педографии – измерения распределения плантарного давления в статике и динамике. Данный метод активно используется для обследования больных сахарным диабетом с синдромом диабетической стопы [3], при изучении особенностей походки пациентов, перенесших инсульт, страдающих болезнью Паркинсона. Результаты исследований могут быть полезны в планировании и оценке эффективности реабилитационных мероприятий [7]. Педографическое обследование больных рассеянным склерозом осуществляется в лаборатории нейроиммунологии Института Мозга человека РАН совместно с ООО «НовелСПб» с 2000 года [1, 5, 6, 9].
Анализ особенностей двигательных нарушений при рассеянном склерозе и оценка влияния на них медикаментозной коррекции и реабилитационных процедур помогут сформировать новые подходы в изучении механизмов двигательных нарушений, расширить возможности диагностики и оптимизировать проводимую терапию, что определяет актуальность настоящего исследования.
Целью работы являлся анализ нарушений походки у больных рассеянным склерозом и возможности медикаментозной коррекции нарушений, связанных с повышением мышечного тонуса в ногах.
Материалы и методы. Анализ особенностей походки при рассеянном склерозе с помощью метода педографии проводился у 95 пациентов. Все обследуемые были разделены на две группы в зависимости от тяжести инвалидизации по шкале Куртцке, им проводился неврологический осмотр и оценивалась тяжесть заболевания по шкалам FS и EDSS.
Характеристика групп пациентов приведена в таблице 1 (группа сравнения – 52 здоровых добровольца (18 мужчин, 34 женщины) в возрасте от 20 до 27 лет).
Таблица 1
Основные данные по количеству пациентов, распределению по полу и возрасту, среднему баллу EDSS и FS
|
EDSS≤1,5 (группа 1) |
EDSS>1,5 (группа 2) |
Число больных (мужчины/женщины) |
34(11/23) |
61(20/41) |
Возраст (годы) |
35±12 |
38±8 |
Средний балл EDSS |
1,2±0,3 |
3,2±1,1 |
Нарушения в пирамидной системе |
1,3±0,6 |
2,5±0,9 |
Нарушения в мозжечковой системе |
1,1±0,4 |
2,3±0,8 |
Часть из обследованных пациентов, у которых отмечался повышенный мышечный тонус в ногах, получала медикаментозную коррекцию препаратом мидокалм. Они были включены в отдельную группу, состоящую из 22 пациентов (10 мужчин и 12 женщин в возрасте от 33 до 49 лет). Инвалидизация больных по шкале EDSS составила от 3 до 6 баллов. У всех пациентов был достоверный рассеянный склероз (согласно критериям Мак-Дональда), ремиттирующий тип течения заболевания (вне обострения). Отсутствовали тяжелые когнитивные нарушения. В зависимости от выраженности мышечного гипертонуса в ногах, все пациенты были разделены на две группы в соответствии со шкалой Эшуорта:
1. С легкой спастичностью (от 1 до 1+ баллов);
2. С выраженной спастичностью (2 и более баллов).
Эти группы пациентов были относительно однородны по полу, возрасту и длительности заболевания, значимые различия имели место в бальной оценке EDSS, FS, что соответствует большей тяжести инвалидизации пациентов 2-й группы. Все пациенты наблюдались амбулаторно.
Общая характеристика групп больных по полу, возрасту, длительности заболевания, тяжести неврологического дефицита и инвалидизации (по шкалам FS, EDSS) представлена в таблице 2.
Таблица 2
Характеристика групп больных, получивших терапию препаратом мидокалм
|
Группа 1 |
Группа 2 |
P |
Число больных (мужчины/женщины) |
9 (5/4) |
7 (3/4) |
|
Возраст (годы) |
41±6 |
41±8 |
|
Длительность заболевания рассеянным склерозом (годы) |
6.9±4.6 |
7±2 |
|
EDSS (баллы) |
3.4±0.5 |
4.9±0.8 |
<0.001 |
Нарушения в пирамидной системе (баллы по FS) |
2.4±0.7 |
2.9±0.4 |
|
Мозжечковые нарушения (баллы по FS) |
1.9±0.6 |
3.1±0.7 |
0.002 |
Спастичность (левая нога) |
0.9±0.4 |
2.1±0.7 |
0.002 |
Спастичность (правая нога) |
1.2±0.3 |
1.5±0.5 |
|
Пациенты, получавшие медикаментозную коррекцию, прошли комплексное неврологическое и нейропсихофизиологическое обследование:
1) неврологический статус и тяжесть инвалидизации оценивались по общепринятым шкалам FS и EDSS (Kurtzke J., 1983);
2) для оценки спастичности (количественная оценка выраженности изменений мышечного тонуса) использовалась шкала Эшуорта;
3) качество жизни оценивалось пациентом с помощью опросника – EuroQol;
4) нарушения распределения плантарного давления оценивались с помощью метода педографии. Измерение осуществлялось с помощью платформы Emed-at 25 system (Novel, Мюнхен, Германия), частота 25 Гц, плотность датчиков – 2 датчика/см2. Использовался протокол “первого шага”, по 5 измерений для левой и правой ног. Измерения проводились до и после курса терапии.
Анализировались следующие параметры: время контакта (мс), пиковое и среднее давления (кПа), максимальная сила (в % к весу тела), интегралы»давление-время» (кПа*с) и»сила-время» (в % к весу тела*с). Для хранения и анализа анамнестических данных, результатов оценки EDSS и FS, результатов осмотра стоп, измеренных данных, расcчитанных параметров распределения давления и определения анатомических областей стопы использовалось программное обеспечение, разработанное Novel.
Неврологический статус, мышечный тонус оценивались до начала терапии в процессе титрации дозы мидокалма и по окончании курса лечения в подобранной дозе (1 мес), педографическое обследование проводилось дважды: до лечения и после окончания курса терапии.
Для сравнения между группами использовался однофакторный анализ ANOVA.
Группе пациентов с повышенным мышечным тонусом в ногах с целью коррекции этих нарушений был назначен мидокалм. Данный препарат был выбран нами за выраженный антиспастический эффект, хорошую переносимость даже в высоких суточных дозировках и при длительном приеме, отсутствие привыкания, отсутствие седативного эффекта и влияния на координацию движений, что, безусловно, является важным у данной группы пациентов.
Результаты и их обсуждение. В таблице 3 приведены значимые отличия в параметрах распределения давления для двух групп больных рассеянным склерозом в сравнении с параметрами давления контрольной группы.
Таблица3
Значимые отличия (р<0.001) в параметрах распределения плантарного давления в группах больных с EDSS≤1,5 (34 пациента) и EDSS>1,5 (61 пациент) в сравнении со здоровыми добровольцами
Параметр |
Отдел стопы |
EDSS≤1,5 |
EDSS>1,5 |
Здоровые добровольцы |
Пиковое давление (кПа) |
Пятка |
292±108 |
260±110 |
334±80 |
|
ПГ(плюсневая головка)2 |
321±144 |
270±94 |
365±132 |
|
ПГ3 |
305±136 |
266±103 |
349±111 |
Среднее давление (кПа) |
Пятка |
141±35 |
131±39 |
|
|
ПГ2 |
150±41 |
139±38 |
|
Максимальная сила (% к весу тела) |
Пятка |
67±15 |
62±18 |
76±11 |
|
Средний отдел |
20±12 |
17±12 |
19±7 |
|
ПГ2 |
24±6 |
21±6 |
25±6 |
Интеграл»давление-время» (кПа*сек) |
ПГ2 |
148±70 |
134±52 |
130±46 |
|
ПГ5 |
77±63 |
95±90 |
82±64 |
|
2 палец |
61±41 |
77±77 |
47±30 |
Интеграл»сила-время» (% к весу тела*сек) |
2 палец |
2±1 |
2±2 |
8±5 |
Время контакта (мс) |
ПГ5 |
849±197 |
915±301 |
690±100 |
Время контакта (% к времени переката) |
ПГ5 |
73±9 |
75±9 |
74±6 |
|
2 палец |
62±15 |
66±18 |
57±14 |
Начало контакта (% к времени переката) |
ПГ1 |
17±8 |
15±10 |
19±6 |
|
ПГ4 |
11±4 |
9±5 |
12±4 |
|
ПГ5 |
14±6 |
12±6 |
13±4 |
|
2 палец |
37±15 |
33±17 |
43±13 |
Площадь контакта (см2) |
Средний отдел |
25±10 |
22±10 |
27±4 |
|
2 палец |
4±1 |
4±2 |
4±1 |
Усредненные картины распределения плантарного давления для сравниваемых групп представлены на рисунке 1.
EDSS≤1.5 EDSS>1.5
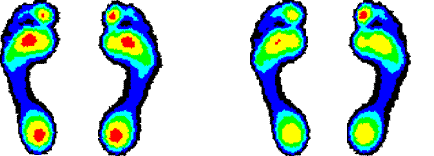
Здоровые добровольцы
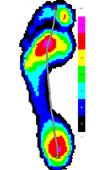
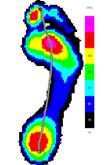
Рис.1. Усредненные картины распределения плантарного давления в сравнении с контрольной группой.
На основании полученных данных можно дать следующую характеристику походки пациентов, страдающих рассеянным склерозом, с различной степенью инвалидизации:
1. Походка пациентов с минимальной степенью инвалидизации (EDSS≤1.5) практически не отличается от походки здоровых пациентов.
2. Для пациентов с умеренным неврологическим дефицитом характерно замедление походки, о чем свидетельствуют параметры, характеризующие время контакта. Кроме того, снижена нагрузка на пятку и центральные плюсневые головки.
Группа пациентов с повышенным мышечным тонусом в ногах получала антиспастическую терапию. Начальная доза мидокалма для всей группы больных составила 50 мг 3 раза в сутки (низкая начальная доза связана с теоретической возможностью развития мышечной слабости и других побочных эффектов, описанных в литературе). Титрация дозы препарата проводилась с учетом того, что спастичность могла компенсировать парез нижних конечностей, и в каждом конкретном случае необходимо было найти баланс между слабостью мышц и спастичностью, позволяющей максимально реализовать двигательную функцию.
В процессе лечения пациентов препаратом Мидокалм минимальная эффективная доза, вызывающая клинический эффект, составила 100 мг в сутки у одного пациента. Попытка увеличения дозы приводила к развитию мышечной слабости. Максимальная эффективная доза - 600 мг в сутки. На этой дозе отмечалось отсутствие спастичности без нарастания мышечной слабости. Средняя эффективная доза составила 450мг в сутки.
На фоне проведенной терапии выраженность неврологических симптомов по шкале FS и тяжесть инвалидизации по шкале EDSS до и после лечения не изменились.
До лечения в группе обследованных больных повышение мышечного тонуса легкой степени (до 2 баллов) наблюдалась у 9 пациентов, что соответствует 56% случаев, выраженная спастичность (2 и более баллов) - у 7 пациентов (44%). После лечения доля пациентов с легкой степенью спастичности увеличилась и составила 94% - 15 человек (из них у 5 пациентов спастичность полностью отсутствовала на обеих ногах после курса лечения, что соответствовало 31,3% от общего числа пациентов), а спастичность 2 и более баллов - у 6% (1 больной) (рисунок 2).
. 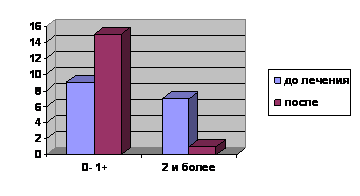
Рис.2. Доля пациентов с различной спастичностью до и после лечения.
При анализе данных визуально-аналоговой шкалы EuroQol, по которой пациенты самостоятельно оценивали состояние своего здоровья, выявлен значительный рост среднего балла через 2 месяца терапии с 56,9 до 62,5, свидетельствующий об улучшении субъективного восприятия больными своего самочувствия.
У большинства пациентов до начала приема мидокалма отмечалось нарушение функции тазовых органов в виде задержки или недержания мочи. Даже при приеме максимальных доз препарат влияния на функцию тазовых органов не оказал.
Из анализа результатов были исключены 6 пациентов:
- у одного пациента на 9-й день приема мидокалма развилась аллергическая реакция, проявившаяся в виде сыпи, отека кистей рук и стоп, отечности лица;
- 1 пациент был исключен из исследования в связи с развившимся обострением заболевания и необходимостью экстренной госпитализации для проведения курса пульс-терапии метилпреднизолоном;
- у 2-х пациентов после приема первых доз препарата развился адбоминальный дискомфорт – пациенты от приема препарата отказались;
- 2 пациентки получили полный курс лечения, но от заключительного обследования отказались.
Все пациенты, получавшие антиспастическую терапию, прошли педографическое обследование до и после курса лечения. Основной задачей обследования было оценить эффективность терапии с помощью данного метода.
На начальном этапе были проанализированы основные значимые параметры распределения давления в сравниваемых группах до начала лечения, результаты приведены в таблице 4.
Таблица 4
Значимые отличия (р<0.001) в параметрах распределения плантарного давления в группах больных до начала терапии
Параметры |
Отдел стопы |
Группа 1 |
Группа 2 |
Пиковое давление (кПа) |
Внешняя часть пятки |
256±71 |
216±77 |
|
Внутренняя часть среднего отдела стопы |
78±42 |
53±33 |
Среднее давление (кПа) |
Пятка |
144±33 |
122±39 |
Максимальная сила (% к весу тела) |
Пятка |
71±15 |
60±20 |
|
Второй палец |
6±3 |
4±3 |
Интеграл «давление-время» (кПа*с) |
ПГ1 |
105±62 |
157±118 |
|
ПГ2 |
125±36 |
155±67 |
|
ПГ3 |
127±39 |
161±54 |
Интеграл «сила-время» (% к весу тела) |
Стопа |
92±16 |
108±19 |
|
ПГ1 |
9±5 |
13±8 |
|
ПГ2 |
10±3 |
13±6 |
|
ПГ3 |
12±4 |
14±4 |
Время контакта (мс) |
Стопа |
1079±161 |
1390±355 |
Основные отличия параметров распределения давления в группе 1 по сравнению с данными группы 2 до лечения состояли в следующем:
1. Время контакта значительно ниже.
2. Пиковое и среднее давление, а также максимальная сила в области пятки значительно выше.
3. Интегралы «давление-время» и «сила-время» в области 1-ой, 2-ой и 3-ей плюсневых головок стопы значимо меньше; интеграл «сила-время» – меньше для всей стопы.
На втором этапе исследования был проведен анализ влияния антиспастической терапии на пациентов из каждой группы отдельно. В таблице 5 приведены значимо отличающиеся параметры распределения давления в группе 1 до и после лечения.
Таблица 5
Сравнительные данные параметров в группе 1 до и после лечения
Параметры |
Отдел стопы |
До лечения |
После лечения |
Р-значение |
Максимальная сила (% к весу тела) |
Стопа |
127±5 |
123±5 |
<0.001 |
Интеграл «давление-время» (кПа*с) |
Пятка |
117±40 |
102±31 |
<0.01 |
|
2 палец |
78±61 |
54±25 |
<0.001 |
|
3,4,5 пальцы |
74±74 |
50±42 |
<0.01 |
Интеграл «сила-время» |
Стопа |
92±16 |
83±13 |
<0.005 |
|
2 палец |
2±1 |
2±1 |
<0.005 |
|
3,4,5 пальцы |
3±3 |
2±1 |
<0.005 |
Время контакта (мс) |
Стопа |
1079±161 |
1017±138 |
<0.005 |
|
Пятка |
746±150 |
681±124 |
<0.005 |
|
Средний отдел |
698±158 |
616±142 |
<0.001 |
|
ПГ2 |
851±141 |
793±109 |
<0.005 |
|
ПГ3 |
886±147 |
822±119 |
<0.005 |
|
ПГ4 |
886±144 |
815±112 |
<0.001 |
|
ПГ5 |
806±152 |
735±110 |
<0.005 |
В группе 1 после лечения отмечалось:
1. Значимое уменьшение времени контакта под всей стопой, а также практически под всеми анатомическими областями стопы, кроме ПГ1 и пальцев (т.е. скорость переноса веса тела значительно увеличилась после лечения.)
2. Значимое уменьшение под стопой - максимальной силы и интеграла «сила-время»; под 2 и латеральными пальцами – интегралов «давление-время» и «сила-время»; под пяткой – интеграла «давление-время». (Может быть объяснено уменьшением времени контакта между стопой и поверхностью при ходьбе).
Параметры распределения давления в группе 2 до и после лечения приведены в таблице 6.
Таблица 6
Сравнительные данные параметров в группе 2 до и после лечения
Параметры |
Отдел стопы |
До лечения |
После лечения |
Р-значение |
Максимальная сила (% к весу тела) |
Стопа |
126±10 |
118±9 |
<0.001 |
|
Пятка |
60±20 |
46±14 |
<0.01 |
Интеграл «сила-время» (% к весу тела) |
ПГ2 |
13±6 |
18±8 |
<0.005 |
|
ПГ3 |
14±4 |
18±5 |
<0.005 |
В группе 2 после лечения отмечалось уменьшение максимальной силы как под всей областью стопы, так и под пяткой, значимое увеличение интеграла «сила-время» под 2 и 3 плюсневыми головками.
Усредненные картины распределения плантарного давления для сравниваемых групп представлены на рисунке 3.
До лечения После лечения
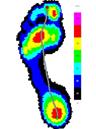
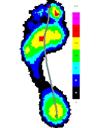
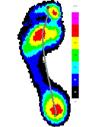
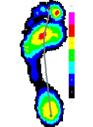
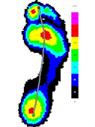
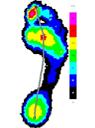
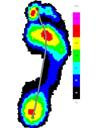
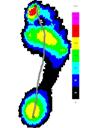
Группа 1 Группа 2 Группа 1 Группа 2
Рис.3. Усредненные картины распределения плантарного давления до и после лечения.
Ниже приведены клинические примеры пациентов из обеих групп.
1. Больной Я., 32 г., пациент из первой группы. EDSS=3,5 балла, нарушения в пирамидной системе - 1 балл, в мозжечковой - 2 балла. Спастичность на обеих ногах до лечения соответствовала 1 баллу по шкале Эшуорта; после лечения спастичность на левой ноге отсутствовала, а на правой сохранилась на том же уровне, что и до лечения. Анализ данных педографии показал, что у пациента значимо увеличилась скорость ходьбы за счет уменьшения времени контакта.
До лечения После лечения
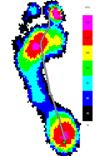
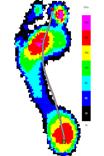
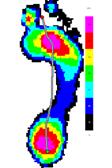
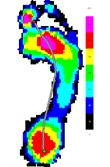
Рис.4. Усредненные картины распределения давления у больного Я., 32 г., до и после лечения в сравнении со здоровыми сверстниками.
На представленных ниже диаграммах можно отметить, что время контакта (рис. 5а) и пиковое давление (рис. 5б) до и после лечения соответствовало нормальным показателям (сравнение с группой здоровых добровольцев); значимые отличия после лечения наблюдаются только в скорости ходьбы (контактное время после лечения значимо уменьшилось).
До лечения После лечения
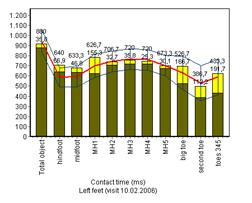 а
а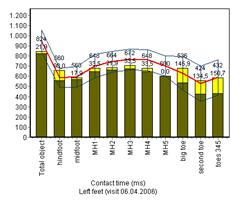
До лечения После лечения
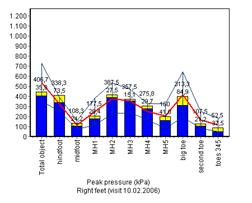 б
б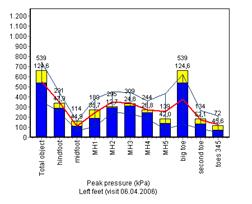
Рис.5. Время контакта и пиковое давление до и после лечения в сравнении с данными здоровых добровольцев.
2. Больная Ц., 38 лет, пациентка из второй группы. Результаты неврологического осмотра: EDSS=4,5, нарушения в пирамидной и мозжечковой системах 3 балла, спастичность по шкале Эшуорта до лечения составляла на левой ноге 2, а на правой - 1 балл соответственно, после лечения спастичность отсутствовала на обеих ногах. При анализе результатов педографического обследования до и после лечения значимые отличия (p<0.001) были получены для времени контакта (до лечения оно составляло 1144±91 мс, а после лечения - 984±87 мс).
На рисунке 6 представлены усредненные картины распределения давления до и после лечения.
До лечения После лечения
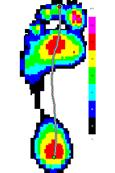
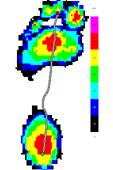
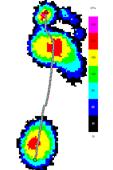
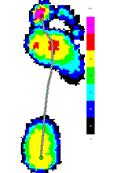
Рис.6. Усредненные картины распределения давления у больной Ц., 38 лет, до и после лечения.
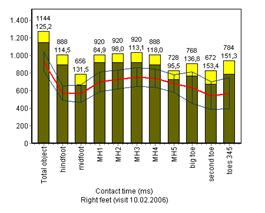
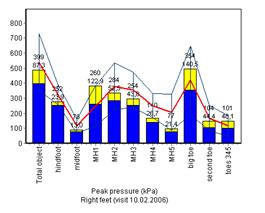
На представленных ниже диаграммах видно, что время контакта (рис.7а) до лечения было выше в сравнении с группой здоровых добровольцев, после лечения данный показатель значимо снизился и приблизился к среднестатистическим показателям здоровых молодых людей. На диаграммах пикового давления (рис.7б) до и после лечения отмечалось снижение показателей пикового давления под всеми областями стопы по сравнению со среднестатистическими показателями здоровых добровольцев; после курса терапии данные показатели значимо не изменились.
До лечения После лечения
 а
а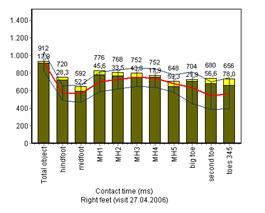
До лечения После лечения
 б
б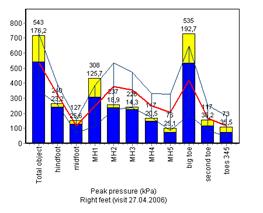
Рис.7. Время контакта и пиковое давление до и после лечения в сравнении с данными здоровых сверстников.
Выводы. Метод педографии является объективным методом оценки степени двигательных нарушений при рассеянном склерозе, позволяющий получить количественные и качественные характеристики ходьбы. Чувствительными параметрами распределения давления, характерными для больных с рассеянным склерозом, являются показатели пикового, среднего давления и максимальная сила под центральными плюсневыми головками, а также время контакта. Для пациентов с умеренным неврологическим дефицитом (EDSS>1,5) характерны увеличение времени контакта (уменьшение скорости ходьбы), снижение давления под пяткой и центральными плюсневыми головками. Основные параметры ходьбы у пациентов с минимальной степенью инвалидизации (EDSS≤1,5) по данным педографии значимо не отличались от показателей у здоровых добровольцев.
Применение препарата Мидокалм с целью коррекции спастичности безопасно и эффективно у пациентов с рассеянным склерозом. В целом, переносимость Мидокалма в обследованной группе была удовлетворительной. На фоне приема Мидокалма у всех обследованных больных выявлено значимое снижение мышечного тонуса в среднем на 1 балл по шкале Эшуорта. При этом у больных с легкой степенью спастичности отмечено увеличение скорости ходьбы. В группе с выраженным повышением мышечного тонуса удалось достичь значимого уменьшения спастичности, что подтверждается клинически и педографически (значимое увеличение давления в области 2 и 3 плюсневых головок) однако, скорость ходьбы не изменилась, что, вероятнее всего, связано с большей выраженностью парезов, координаторных и чувствительных нарушений и, в целом, с большей тяжестью заболевания.
Учитывая, что после коррекции спастичности, атаксия заняла одно из ведущих мест в картине двигательных нарушений, можно сделать вывод о том, что назначение антиспастических препаратов является лишь частью комплексной терапии у больных рассеянным склерозом с высокой степенью инвалидизации. Применение таблетированных форм Мидокалма у больных рассеянным склерозом не оказывает влияния на тазовые функции. Качество жизни пациентов на фоне проводимой терапии улучшилось. Данный препарат может быть рекомендован для терапии спастичности пациентов с рассеянным склерозом.
Список литературы